近日,我院周昕研究员团队在国际顶级科技期刊《Advanced Science》发表了题为《Engineering Dimensional Configuration of Single-Atom S-Cu-S Sites as Reversible Electron Station for Enhanced Peroxidase-Mimicking》的研究论文,设计并合成了具有模拟天然酶3D催化口袋构型的铜单元子类过氧化物酶MoCC,其催化性能相比天然辣根过氧化物酶在H2O2底物上的最大反应速度(Vmax)提升约16.3倍,亲和力提高约17.9倍,比活力(Specific activity)高1.2倍。
新兴的金属单原子纳米催化剂(SAzymes)已受到广泛关注,特别是在治疗耐药细菌感染方面。与传统纳米催化剂相比,SAzymes具有更优异的催化活性,这是由于其最大化的原子利用率以及明确的电子、几何结构。此外,SAzymes的金属活性位点可以通过调节金属-支撑相互作用、结构-活性关系及定制表面改性、配位数和元素、缺陷等物理化学性能精细调控。
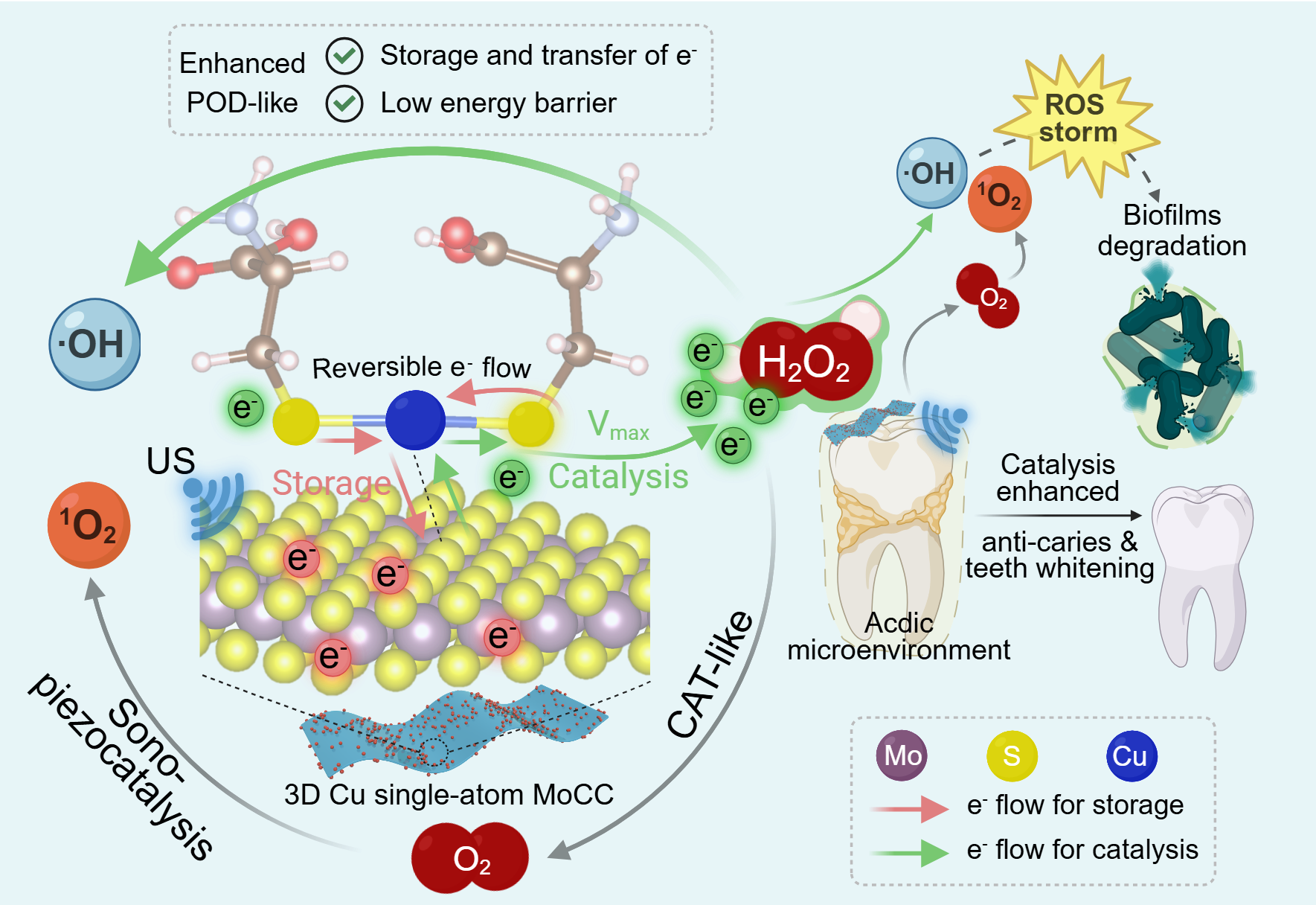
基于上述背景,受片状硫化钼(MoS2)的特点以及天然酶催化口袋的启发,本研究创新性地提出了具有模拟天然酶3D催化口袋构型的铜单元子类过氧化物酶MoCC Sazymes。通过半胱氨酸(L-Cys)配位触发的自组装过程,将单原子活性中心S-Cu-S三维定位在MoS2平面上。通过调节Cu与MoS2的比例,实现了最大10.11%的铜单原子负载率。MoCC的POD-Like活性与级联产生的过氧化氢酶(CAT)活性可以在细菌感染部位催化产生显著的活性自由基·OH和1O2的生成。动物试验结果显示,MoCC催化产生的自由基风暴可以有效清除生物被膜并杀死病原微生物,并且保证了良好的生物安全活性。
本研究提出的氨基酸驱动的自组装纳米催化剂实现了活性位点与天然酶三维催化口袋之间的最佳匹配。这些由L-半胱氨酸稳定的S-Cu-S催化位点能够在耐药菌感染的病灶微环境中高效催化H2O2分解,产生自由基风暴,并选择性地高效清除病原微生物。本研究为设计超越天然酶的治疗性纳米催化剂提供了一种独特策略,并为增强抗菌感染效果提供了宝贵的见解。
扬州大学兽医学院周昕研究员为共同通讯作者,2023级博士研究生马文杰为第一作者,扬州大学与中科院高能物理研究所(IHEP)为共同通讯单位,该研究工作得到了国家重点研发等项目支持。