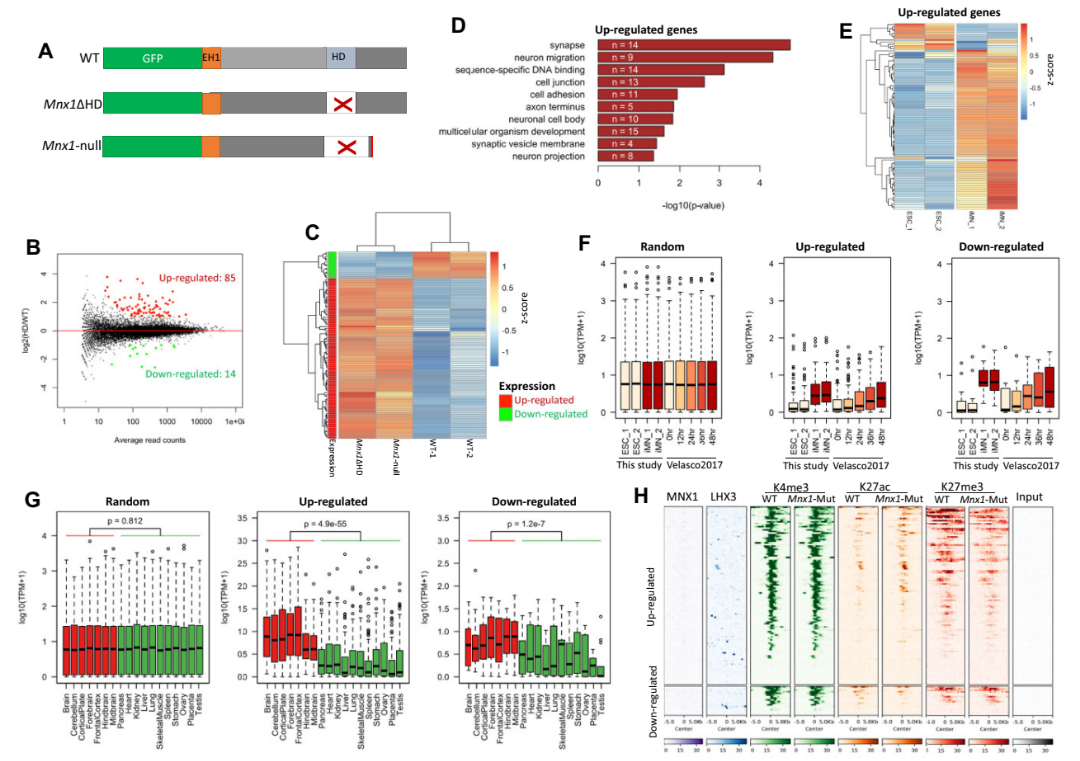
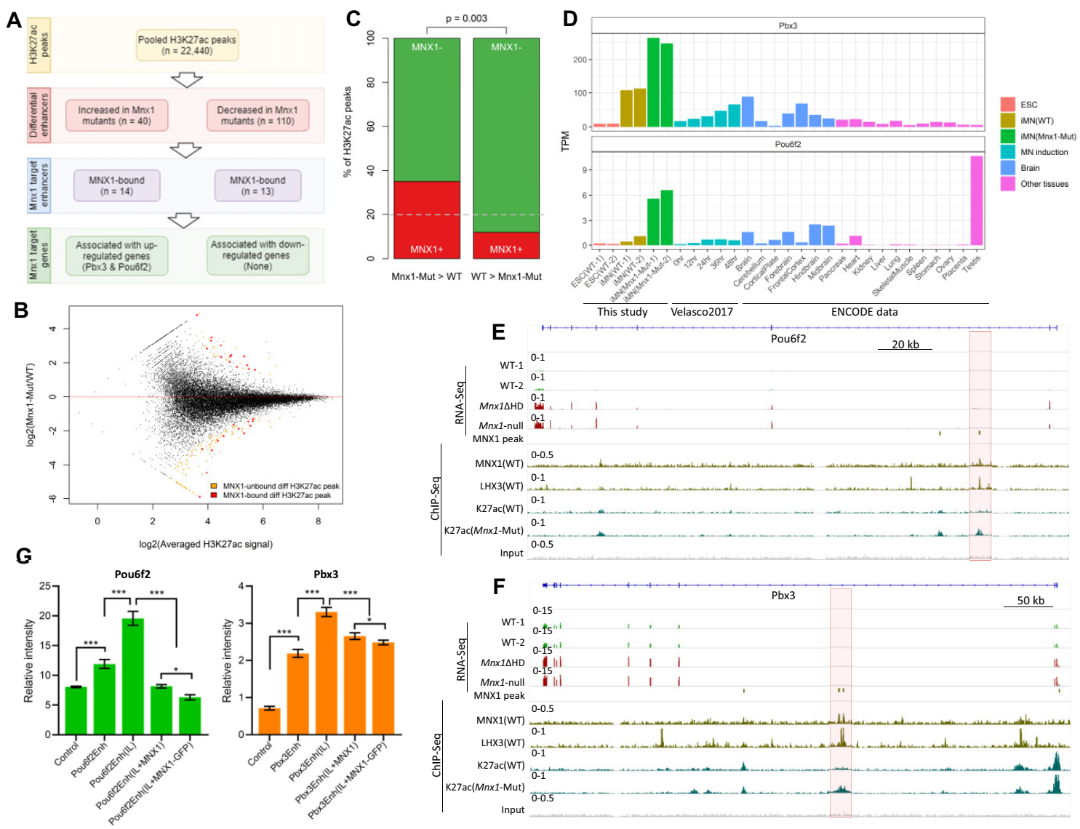
近日,我院孙名安教授课题组与美国国立卫生研究院Todd Macfarlan课题组在《Nucleic Acids Research》在线发表题为“The homeobox transcription factor MNX1 regulates the expression of many non-MN-specific neuronal genes in motor neurons”的研究论文,应用运动神经诱导模型并整合组学与实验手段,针对MNX1的功能及调控机制进行了研究。本研究发现在运动神经中,MNX1通过直接结合并抑制Pou6f2与Pbx3等少数基因,来影响大量本应在中枢神经系统中广谱表达的基因的表达水平。
扬州大学是本研究成果的第一完成单位,扬州大学孙名安教授与美国国立卫生研究院Todd Macfarlan研究员为并列通讯作者。孙名安教授、范海瑞博士后、Sherry Ralls博士为并列第一作者,在读博士蒋佳瑶参与了本研究。本研究得到国家自然科学基金(31900422)、江苏“特聘教授”等项目的资助。
该研究首先对以往的运动神经诱导模型进行优化,实现了胚胎干细胞到运动神经的高效诱导分化。随后应用ChIP-seq技术并整合表观组数据,对MNX1在运动神经中的结合分布模式进行了解析。接着,应用CRISPR技术对MNX1进行敲除,并应用转录组与表观组技术对其调控的基因与位点进行研究。最后,对MNX1缺失后H3K27ac的差异分布情况进行挖掘,并同差异表达的基因进行了比较,以基对MNX1直接调控的位点和基因进行鉴定。
Homeobox家族转录因子在发育与细胞分化过程中起到重要作用。本研究聚焦MNX1这一运动神经中特异表达的homeobox蛋白开展研究,揭示了其在运动神经中对大量神经基因的调控功能,进而发现其可能通过对Pou6f2与Pbx3等极少数基因的结合调控,影响其它许多本应在中枢神经系统中普遍表达的基因的转录水平。该成果首次系统阐明了MNX1在运动神经中的功能与调控机制,加深了对MNX1蛋白功能以及运动神经特性的理解。此外,该成果对homeobox蛋白转录调控模式的理解也具有一定意义。