近日,我院朱建中教授团队在《Cell Reports》期刊发表题为“Porcine IRF2 suppresses the cGAS-STING-mediated antiviral IFN signaling by competing IRF3 for binding to the IFN promoter”的研究论文。该研究首次系统阐明了猪源IRF2(pIRF2)作为cGAS-STING通路的负调控因子,填补了IRF家族在抗病毒信号转导中的知识空白,为理解免疫平衡提供了新视角。
面对非洲猪瘟(ASFV)、猪伪狂犬病(PRV)等猪病毒疫病,先天免疫系统是宿主抵御其入侵的关键防线,其中cGAS-STING-IRF3-IFN信号通路在识别细胞质中病毒DNA并触发干扰素抗病毒反应中扮演核心角色。干扰素调节因子(IRF)家族成员如IRF3已知参与该通路的转录激活,但其它IRF家族成员蛋白的功能尚不明确。
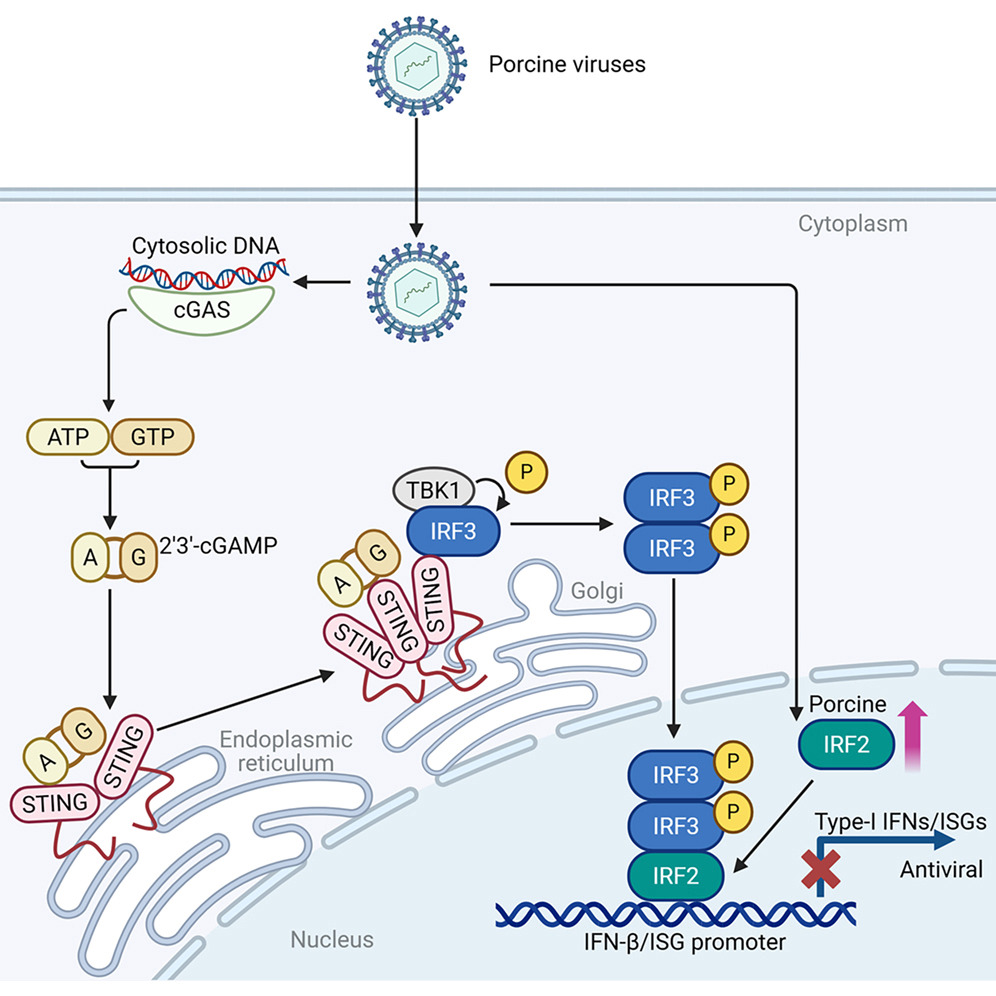
研究采用双重筛选系统,即在猪源IRF敲除细胞中和转染表达细胞中分别筛查各IRF成员,发现pIRF2对IFN-β启动子活性的抑制作用。研究表明,pIRF2的抑制功能依赖于其DNA结合结构域(DBD),而非IRF关联结构域(IAD)。实验证实,pIRF2可直接结合IFN-β启动子的干扰素刺激反应元件(ISRE),并与IRF3竞争性占据相同结合位点,从而阻断IRF3介导的转录激活。这种“基因占位”策略类似于IRF2对IRF1的已知拮抗作用,但本研究首次揭示其在cGAS-STING通路中的特异性功能。此外,pIRF2对ISG启动子也表现出结合能力,表明其调控范围可能扩展至多个干扰素相关靶点。尽管目前在活猪体内直接进行基因干预尚存技术和伦理挑战,但pIRF2作为天然免疫的关键“刹车”,已成为开发新型免疫调节剂、提高猪群基础免疫力的重要潜在靶点。
兽医学院博士后姜森为第一作者,朱建中教授为通讯作者。该研究工作获得了国家自然科学基金等相关科研项目资助。